检测意义
宿主细胞外源核酸污染,DNA是主要污染源,具有潜在的理论风险(如致癌性、传染性),而RNA被认为风险极低,通常会迅速降解并被人体内的核糖核酸酶清除。美国FDA、欧洲EMA和中国NMPA都要求对细胞来源杂质有明确的检测要求[1-5]。
有文献报道先天免疫系统识别DNA和RNA的机制,通常是经过TLR和非TLR途径。RNA免疫的核心机制在于模式识别受体(Pattern Recognition Receptors, PRRs) 如何识别外源核酸并激活先天免疫反应。模式识别受体(PRRs)的免疫生物学对控制病原体感染,尤其是RNA病毒感染至关重要。RNA模式识别受体主要包括TLR3、TLR7、TLR8、RIG-I、MDA5、NLRP3、NOD2以及其他少数受体,见图1。其中,TLR7 和 TLR8,识别单链RNA (ssRNA);TLR3识别双链RNA(dsRNA)。RIG-I和MDA5识别细胞质中的病毒RNA(短链dsRNA带有5'三磷酸末端或长链dsRNA)。RIG-I样受体位于细胞质中,是抗病毒免疫的关键传感器[6]。
同时RNA也有类似于mRNA的作用,即进入体内,翻译并呈递到细胞表面的作用[7],见图2。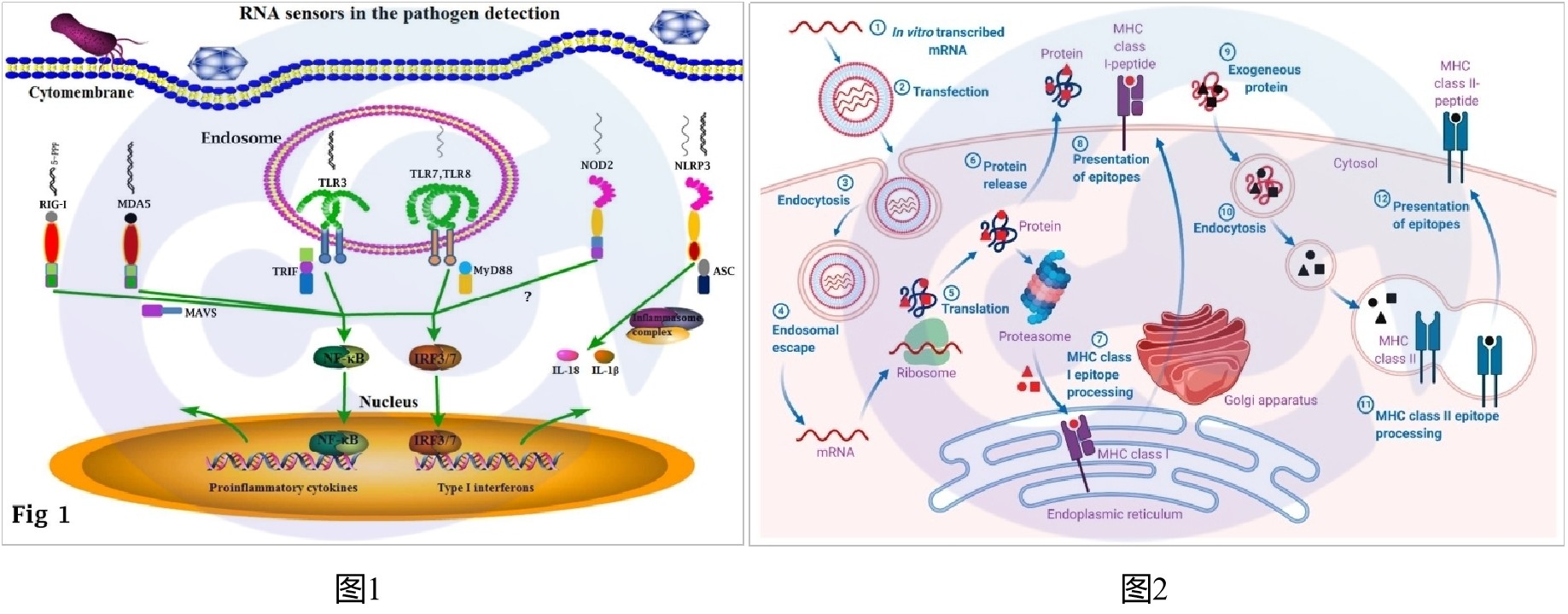
监管要求
因为哺乳动物自身RNA都是经过修饰的(如甲基化),并且通常被限制在特定的细胞器内,从而与这些受体隔离,避免了自身免疫反应。而细菌、病毒来源的RNA缺乏这些修饰,因此容易被识别为“非我”。
这些外源RNA结合受体,通常在免疫细胞(如浆细胞样树突状细胞、巨噬细胞)的内体中被激活,并导致I型干扰素(IFN-α/β)和大量炎性细胞因子(如TNF-α, IL-6)的产生和释放。这可能引起,如发烧、寒战、头痛、肌肉酸痛等流感样症状。
这种由强烈的、系统性的炎症反应介导,理论上可能导致细胞因子风暴等严重毒性,但这需要非常大量的外源RNA,在纯化后的生物制品中虽然不可能达到强烈的免疫原水平。
但是,在特定情况下,持续或反复的免疫激活最终可能导致免疫抑制或耗竭,但这同样需要极高的暴露水平。
因此,监管机构会逐步加强这类杂质的工艺清除验证。稳定地将DNA和HCP清除到合格水平,被控制在可接受的范围内。
综上,根据目前监管要求,和未来监管趋势。赛唐生物体系化地开发了E.coli细胞来源杂质(蛋白/DNA/RNA)系列产品,见表1。及其相关数据,见图3,表2-3。力争为生物药物杂质检测做到全面保障。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 宿主RNA | E.coli 总RNA QPCR | EC-R100T | 0.002-20pg/uL |
|
|
|
|
|
|
|
|
|
|
表1
数据处理
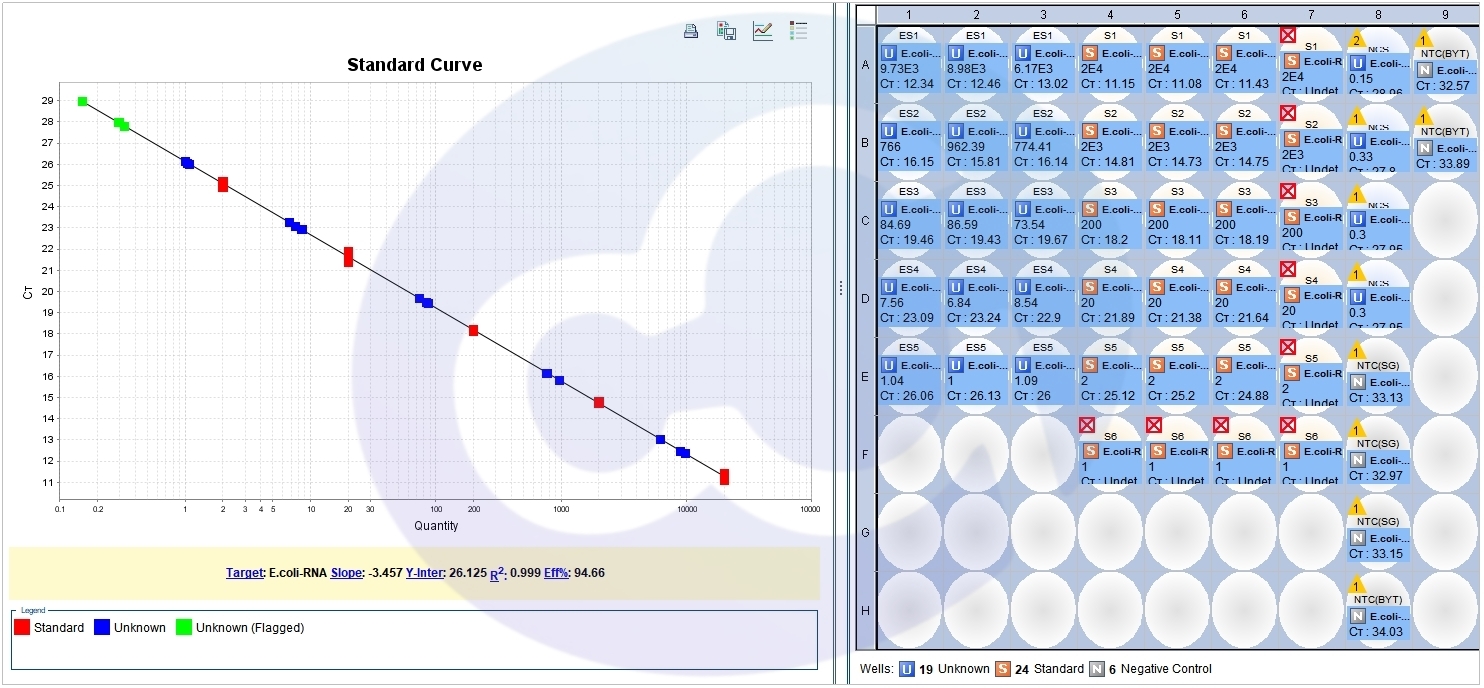
图3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
表2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
表3
Reference:
[1]ICH Q6B:Specifications: Test Procedures and Acceptance Criteria for Biotechnological/Biological Products.
[2]ICH Q7:Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients.
[3]USP:<1130> Nucleic Acid-Based Techniques;<508> Residual Host Cell Protein Measurement.
[4]EP:2.6.7. Nucleic acid amplification techniques ; 5.2.3. Cell substrates for the production of vaccines for human use.
[5]ChP:《生物制品生产用原材料及辅料质量控制》、《人用重组DNA蛋白制品总论》.
[6]Nanhua Chen, et al. RNA sensors of the innate immune system and their detection of pathogens. IUBMB Life. 2017. 69(5):297-304.
[7]Abishek Wadhwa, et al. Opportunities and Challenges in the Delivery of mRNA-based Vaccines. Pharmaceutics. 2020. 12(2):102.
